翰宇药业利拉鲁肽注射液获美国FDA暂定批准
小微
2024月06月24日
阅读数 68138
中国网财经6月24日讯 日前,翰宇药业公告称,公司近日收到美国食品药品监督管理局(下称“FDA”)的通知,由翰宇药业及 Hikma Pharmaceuticals USA,Inc.联合向FDA申报的利拉鲁肽注射液新药简略申请(ANDA,即美国仿制药申请)已获暂定批准。
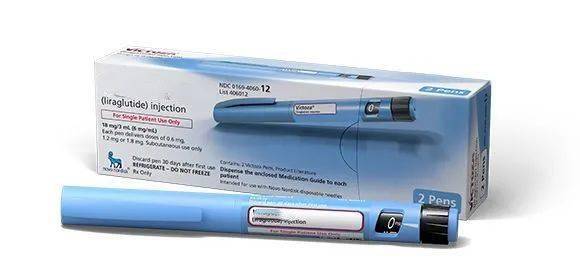
图片来源于网络,如有侵权,请联系删除
据悉,暂定批准是指FDA已经完成仿制药的所有审评要求,即药品经审查,质量、安全和有效性已符合在美国上市的标准,出于专利权和/或独占权(exclusivity)未到期的原因,而给予的一种批准形式。直至专利或独占权问题解决后,美国FDA才能给予在美国终端市场销售的资格。
对此,翰宇药业表示,此次利拉鲁肽注射液获得FDA暂定批准,标志着该产品通过了仿制药的所有审评要求,即药品经审查,质量、安全和有效性已符合在美国上市的标准,有利于 提升公司产品的市场竞争力,对公司拓展美国市场带来积极的影响。
(责任编辑:王晨曦)推荐阅读:
相关文章
- 2024年12月 (15)
- 2024年11月 (24)
- 2024年10月 (32)
- 2024年9月 (183)
- 2024年8月 (212)
- 2024年7月 (286)
- 2024年6月 (349)
- 2024年5月 (308)
- 2024年4月 (366)
- 2024年3月 (389)
- 2024年2月 (168)
- 2024年1月 (223)
- 2023年12月 (77)
- 2023年11月 (16)
- 2023年9月 (2)
- 2023年4月 (5)
- 2023年3月 (3)
- 2023年2月 (5)
- 2023年1月 (1)
- 2022年12月 (10)
- 2022年11月 (12)
- 2022年10月 (14)
- 2022年9月 (7)
- 2022年8月 (9)
- 2022年7月 (1)
- 2022年5月 (4)
- 2022年4月 (1)
- 2022年3月 (2)
- 2022年2月 (2)
- 2021年12月 (2)
- 2021年11月 (1)
- 2021年3月 (2)
- 2020年8月 (1)
- 2020年7月 (1)
- 2020年3月 (2)
- 2020年2月 (3)
- 2017年9月 (6)
- 2017年8月 (12)
热门
- 1 卫龙陷魔芋爽克重不足风波 “减重”又“加价”双双引质疑 中国网财经5月28日讯 近日,知名零食品牌卫龙旗下产品魔芋爽被曝克重不足,标重净含量为15克,实际称重却只有8.9克,且8.9克实际称重包含了包装袋的重量。图片来源于网络,如有侵权,请联系删除 上述消息引发舆论热议,相关词条迅速登...
- 2 移卡公布2024年中期业绩:一站式支付服务收入13.47亿 中国网财经8月27日讯 27日,基于支付的科技平台——移卡有限公司(以下简称“移卡”或“公司”)发布2024年中期业绩报告。报告期内,公司实现收入15.78亿元(人民币,下同):其中一站式支付服务13.47亿元,商户解决方案2.02亿元...
- 3 山西向民间资本推介60个合作项目 计划总投资1925亿元 中国网财经3月26日讯 据山西省发改委网站26日消息,为进一步拓宽民间投资领域,促进民营经济发展壮大,山西省发展改革委按季组织向民间资本推介项目,鼓励民营企业以独资控股参股等形式参与政府和社会资本合作项目。近日,山西省发展改革委会同省交...
- 4 中国农业大学“神农大模型2.0”正式发布 2024年7月13日,在北京举办的第八届智慧农业创新发展国际会议上,中国农业大学农业大模型研究团队发布了重大科研成果——“神农大模型2.0”。这一里程碑式的创新,标志着农业智能化技术的又一次飞跃,将为加快我国农业新质生产力的建设及农业农...
- 5 VC/PE周报丨软银买了家芯片公司;人形机器人再获投资 .u-top-list li { margin-right:0px; } .u-top-list li a{ margin-right:0px; font-si...
- 6 中远通明日上市:公告提示业绩下滑、客户集中度高等风险 中国网财经12月7日讯 中远通昨日晚间发布公告,宣布公司将在12月8日在深交所创业板上市。此次发行价为每股6.87元,新股发行数量7017.5万股,发行后总股本为2.8亿股。图片来源于网络,如有侵权,请联系删除 公告提示,创业板公...
- 7 伯克希尔迎来“后芒格”时代,投资风格要变了? 每经记者 文巧 每经编辑 兰素英 图片来源于网络,如有侵权,请联系删除 图片来源:路透社报道截图图片来源于网络,如有侵权,请联系删除...
- 8 交通运输部:前5月港口外贸货物吞吐量22.2万吨 同比增长8.9% 中国网财经6月26日讯 26日上午,国务院新闻办公室就水运智慧化转型升级及今年中国航海日有关情况举行发布会。交通运输部副部长付绪银在会上介绍,今年1—5月份,水路货运量完成了38.6亿吨,同比增长了7%;港口集装箱吞吐量突破了1.3亿标...
- 9 贵广网络因信披违规被出具警示函 2023年净利润预亏超11.50亿元 中国网财经3月21日讯 3月21日,贵广网络(600996.SH)发布公告显示,公司近日收到中国证监会贵州监管局《关于对贵广网络、李巍、翟海虹、黄宗文采取出具警示函措施的决定》。图片来源于网络,如有侵权,请联系删除 经查,贵广网络...
- 10 行业ETF风向标丨创新药集体大涨走强,港股创新药ETF换手率超100% .u-top-list li { margin-right:0px; } .u-top-list li a{ margin-right:0px; font-si...
随机
推荐
-
【央行:优化现金使用环境 促进支付方式多元化发展】 1年前 (2023-12-29)
-
【华夏理财董事长苑志宏:银行理财在资产配置上具有独特内在逻辑】 1年前 (2023-12-24)
-
【盐湖股份被生态环境部点名:存在超规模开采盐湖资源、违规取水用水等问题】 1年前 (2023-12-04)
-
【宝莱特心电图机被国家药监局通报质量不合格 坦承“属公司低端产品”】 2年前 (2023-11-16)
热评
- 华脉科技5.14亿定增“夭折” 2023年预亏最高超8000万
- 大为股份连拉两涨停后发异动公告:不存在违反信息公平披露情形
- 哈弗H7多次因烧机油被投诉 车主质疑该车存缺陷
- A股五大险企2023年合计实现净利润超1600亿元:寿险新业务价值高增 财险盈利保持稳定
- 钧达股份:上饶基地目前有部分未完结订单仍在生产履行中
- 飞天茅台价格单日暴跌190元 茅台悄然打响“价格保卫战”
- 俞敏洪、董宇辉再合体直播:未回应热点,与辉同行当天GMV超千万元
- 相关资产减值测试不准致多期财报数据有误 西藏天路及两位相关责任人被警示
- 港股9日跌0.0% 收报17523.23点
- ETF今日收评 | 光伏相关ETF涨约5%,影视,传媒、游戏等ETF跌逾2%
 指南财经网
指南财经网