加快拥抱全球市场 国产创新药出海热情澎湃
恒瑞医药GLP-1类创新药组合实现海外许可、基石药业宣布国产PD-L1出海迎重大里程碑、复宏汉霖单抗生物类似药在美获批……近日,国产创新药出海捷报频传。业内专家认为,这是前期中国创新药投资的一次集中回报,海外市场需求也将倒逼国内创新药企加快源头创新,推动产业链优化、竞争力重塑、价值链跃升。

图片来源于网络,如有侵权,请联系删除
出海形式更加多元

图片来源于网络,如有侵权,请联系删除
6月7日,一辆装满复宏汉霖自主研发和生产的汉曲优正式从上海徐汇基地开出,前往沙特阿拉伯,有望成为首个登陆中东市场的国产单抗(单克隆抗体)生物药。这是继该创新药4月底成为首个中国、欧盟、美国三地获批的国产单抗生物类似药后,再次传来的出海好消息。
另一款国产创新药也迎来里程碑。近日,基石药业宣布,其舒格利单抗获得欧洲药品管理局人用药品委员会积极意见,支持其用于转移性非小细胞肺癌。该药不但有望进入欧盟市场,也或将成首个出海成功的国产PD-L1单抗。
国内创新药企出海形式也更加多元化。不久前,恒瑞医药宣布将具有自主知识产权的GLP-1产品组合有偿许可给美国Hercules公司,协议总金额60.35亿美元,不仅刷新今年药企海外商务拓展(BD)合作交易金额纪录,在交易结构上也创造了国内首例——除首付款、里程碑付款、销售分成外,还获得相关公司近20%的股权。
这种合作形式被业内称为对外授权许可(License-out)。记者注意到,2017年至2019年,国产创新药以该形式出海数量每年均不超过10款。随着国内创新药企出海热情高涨,2023年,中国药企对外授权许可数量首次超过授权引进(License-in)。据不完全统计,今年1月至4月,国产创新药对外授权许可项目累计25笔,较去年同期增长56%,累计交易总金额超百亿美元。
东南亚等新兴市场成新选择
如今,越来越多的药企在完成欧美药品认证后,逐渐开始发力布局全球多个新兴市场。
记者获悉,君实生物正计划将其出口美国的特瑞普利单抗以及多款临床候选产品,平移出口到东南亚,已向新加坡、马来西亚等地提交了上市许可申请。2023年10月,特瑞普利单抗获得美国FDA批准,成为首款获得FDA批准的中国自研自产创新生物药。
“国产药企的创新能力强于印度或东南亚企业,这是我们的优势,生物类似药或创新药等专利产品在东南亚的市场空间更大。”君实生物副董事长李宁表示,这也是很多国产药企选择先赴欧美完成高标准注册、再到东南亚等区域上市的原因。
普华永道报告显示,去年中国企业在东南亚医疗市场的直投事件达到13件,较前一年翻番。经过一轮“欧美认证热”的国产生物医药行业,正在上演新版“下南洋”,并通过授权出海、自建渠道等方式,逐步扩大中国药企在新兴国家的品牌影响力。
“做创新药出海,国家选对很重要。”美中医药开发协会中国主席、北京门罗生物科技有限公司董事长兼CEO戴卫国看来,随着最近几年国际环境发生变化,新兴市场成为越来越多公司的选择,“除了东盟外,巴西、俄罗斯等国家,都是颇有潜力的市场。”
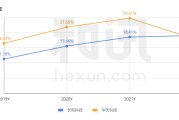
避开竞争激烈的欧美市场也给许多产品市场增长的空间。巴西、印尼、越南、墨西哥等市场的人口基数,奠定了药物未来的产业基础和市场前景。艾昆纬数据显示,2022至2026年,新兴市场医药市场平均5年复合增速为5%至8%,比发达市场要高,不失为性价比之选。
海外市场倒逼源头创新提速
“近段时间以来,‘出海打算’几乎成了投资人的必问题。”一名业内人士对记者表示,对于投入巨大的创新药企来说,“不出海便出局”成了行业共识。
出海之后利润如何?一家药企相关负责人表示,在某些领域已经形成惨烈的价格战,“很多企业可能连研发成本都收不回来。”
“以前做药,是考虑能不能做成,现在做药,还得考虑做成之外,有没有人买单。”戴卫国表示,目前有些创新药尚未上市,便可以通过海外授权的形式出海,“这一新的形势,也对药企出海提出了更高的要求,要选择做最有价值的且有人买单的创新药。”
激烈竞争中,机会仍在源头创新力。“重复性创新的商业空间在缩窄。”在全球健康药物研发中心主任、清华大学药学院创始院长丁胜看来,出海需求正在倒逼国内创新药企加快源头创新,能否做出和别人不一样的地方,决定着药企的长远未来。
(责任编辑:朱赫)推荐阅读:
 指南财经网
指南财经网